Próbna matura 2017. Chemia - sprawdź się!
Zadania w arkuszu maturalnym z chemii na poziomie rozszerzonym mają na celu sprawdzenie:
- umiejętności rozumowania, argumentowania i wnioskowania
- umiejętności wykorzystywania informacji z różnorodnych źródeł
- umiejętności projektowania doświadczeń chemicznych i interpretowania wyników
- umiejętności wykorzystywania narzędzi matematycznych do opisu i analizy zjawisk i procesów
PRÓBNA MATURA 2017 Z CHEMII
Zadanie 1.
Określ typ hybrydyzacji orbitali atomu węgla w cząsteczkach związków, których wzory podano poniżej. Uzupełnij tabelę.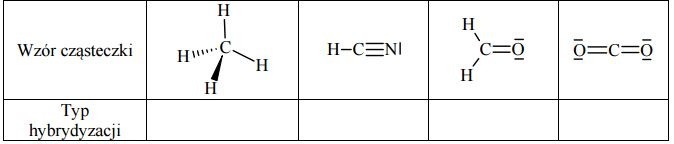
Zadanie 2.
Wypełnij tabelę, wpisując literę P, jeżeli zdanie jest prawdziwe, lub literę F, jeśli jest fałszywe.
1. Typ hybrydyzacji orbitali atomu azotu w cząsteczce amoniaku jest taki sam, jak typ hybrydyzacji orbitali atomu węgla w cząsteczce metanolu. P/F
2. Hybrydyzację, w której uczestniczą jeden orbital s oraz dwa orbitale p, nazywamy hybrydyzacją sp3 (tetraedryczną). P/F
3. Kształt cząsteczki tlenku węgla(IV) wynika z liniowego ułożenia zhybrydyzowanych orbitali atomowych węgla. P/F
Zadanie 3.
Zadanie 4.
Kryształy metali i ich stopów mają postać sieci przestrzennych. Węzły tych sieci obsadzone są kationami metali, w tym przypadku nazywanymi rdzeniami (zrębami) atomowymi. Metale tworzą sieci różnego rodzaju. Metale, które tworzą taki sam rodzaj sieci, różnią się wartościami stałej sieciowej a, czyli odległościami pomiędzy środkami sąsiadujących rdzeni atomowych. Poniżej przedstawiono wartości stałej sieciowej a wybranych litowców i berylowców.
a) Na podstawie podanych informacji określ, który spośród wymienionych w tabeli berylowców charakteryzuje się najwyższą temperaturą topnienia. Uzasadnij swój wybór.
Najwyższą temperaturą topnienia charakteryzuje się: ……
Uzasadnienie: ……
b) Uzupełnij poniższe zdanie, podkreślając te określenia spośród oznaczonych literami A–F, które pozwolą utworzyć poprawny wniosek.
A. mniej
B. więcej
C. mniejszą
D. większą
E. niższa
F. wyższa
Wapń w porównaniu z cezem ma ( A. / B. ) elektronów walencyjnych i ( C. / D. ) wartość stałej sieciowej a, dlatego temperatura topnienia wapnia jest ( E. / F. ) niż cezu.
Informacja do zadań 5–7.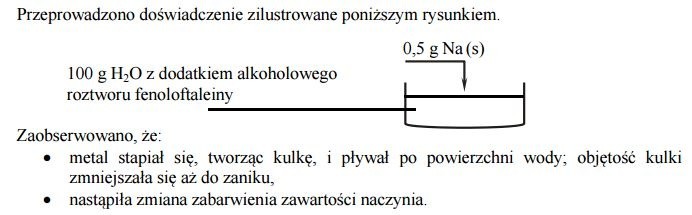
Zadanie 5.
a) Uzupełnij opis przebiegu doświadczenia. Podkreśl T (tak), jeśli obserwacja jest prawdziwa, lub N (nie) – jeśli jest nieprawdziwa.
Wytrącił się biały osad. T/N
Wydzielił się bezbarwny gaz. T/N
b) Dokończ zdanie, podkreślając wniosek A. albo B. i jego uzasadnienie 1. albo 2.
Wnioskujemy, że otrzymany w naczyniu roztwór ma odczyn
A. obojętny,
B. zasadowy
ponieważ
1. uległ on odbarwieniu.
2. zabarwił się na malinowo.
Zadanie 6.
Wybierz i podkreśl w tabeli spośród podanych A–F takie dokończenie każdego zdania, aby powstały poprawne wnioski z przeprowadzonego doświadczenia.
A. endoenergetyczna.
B. egzoenergetyczna.
C. wysoką temperaturę topnienia.
D. niską temperaturę topnienia.
E. gęstość większą od gęstości wody.
F. gęstość mniejszą od gęstości wody.
1. Podczas doświadczenia opisanego w informacji przebiega reakcja A. / B.
2. Pływanie metalu po powierzchni wody wskazuje, że ma on C. / D. / E. / F.
Zadanie 7.
Po zakończeniu doświadczenia poproszono uczniów o obliczenie stężenia procentowego otrzymanego roztworu w procentach masowych i podanie wyniku z dokładnością do drugiego miejsca po przecinku. Ustalono (wykonując poprawne obliczenia), że ilość wody biorącej udział w reakcji wynosi 0,39 g, a masa wodoru, który opuścił środowisko reakcji, jest równa 0,02 g. Poniżej przedstawiono rozwiązania pięciu uczniów, które poddano analizie i ocenie.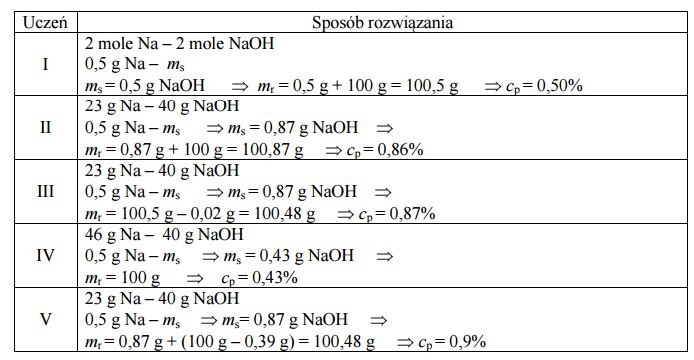
Przeczytaj poniższy tekst. Uzupełnij luki, wpisując numery uczniów (I–V), do których odnoszą się poszczególne stwierdzenia.
Tylko rozwiązanie ucznia oznaczonego numerem ___ nie zawiera błędów. Uczeń ten prawidłowo powiązał dane z szukaną, nie popełnił błędów rachunkowych i podał wynik ze wskazaną dokładnością. Uczeń oznaczony numerem ___ zastosował poprawną metodę rozwiązania zadania, poprawnie wykonał obliczenia, jednak wynik końcowy podał z inną niż wymagana dokładnością. Nieuwzględnienie stechiometrii reakcji oraz niepoprawne wskazanie masy roztworu to błędy, które pojawiły się w rozwiązaniu ucznia oznaczonego numerem ___. W kolejnym rozwiązaniu przy poprawnie obliczonej masie substancji zapisano niepoprawne obliczenia dotyczące masy roztworu. Taki błąd wystąpił podczas rozwiązania zadania przez ucznia oznaczonego numerem ___. Niepoprawnie obliczona masa roztworu oraz błędnie zapisana zależność (proporcja) prowadząca do ustalenia masy substancji nie pozwoliły uczniowi oznaczonemu numerem ___ na zaprezentowanie poprawnego sposobu rozwiązania zadania.
Informacja do zadań 8–10.
Zadanie 8.
Napisz, czy dimeryzacja NO2 jest reakcją egzoenergetyczną, czy endoenergetyczną. Odpowiedź uzasadnij.
Rekcja dimeryzacji NO2 jest reakcją ……
Uzasadnienie: ……
Zadanie 9.
Zadanie 10.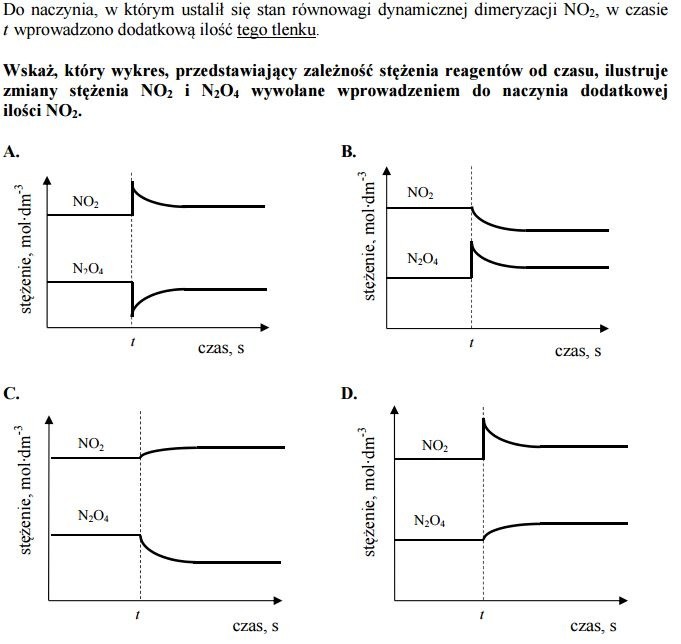
Informacja do zadań 11–13 
Zadanie 11. 
Zadanie 12.
Zapisz w formie cząsteczkowej równanie reakcji zachodzącej w etapie II procesu odsiarczania gazów spalinowych.
Zadanie 13.
Siarczan(VI) wapnia może tworzyć uwodnione kryształy (hydraty). W tabeli podano liczbę moli cząsteczek wody przypadających na jeden mol siarczanu(VI) wapnia (liczbę hydratacji soli) w zależności od zakresu temperatur, w których krystalizuje siarczan(VI) wapnia.
Podaj wzór produktu, który otrzymano po wyprażeniu.
Wzór ……
Zadania pochodzą z informatorów CKE
SPRAWDŹ SWOJE ODPOWIEDZIPróbna matura 2017. Chemia - sprawdziłeś się?
Dołącz do nas na Facebooku!
Publikujemy najciekawsze artykuły, wydarzenia i konkursy. Jesteśmy tam gdzie nasi czytelnicy!
Dołącz do nas na X!
Codziennie informujemy o ciekawostkach i aktualnych wydarzeniach.
Kontakt z redakcją
Byłeś świadkiem ważnego zdarzenia? Widziałeś coś interesującego? Zrobiłeś ciekawe zdjęcie lub wideo?




