Maturę 2017 z chemii zdawać będą uczniowie, którzy chcą studiować medycynę, weterynarię, nauki przyrodnicze lub chemię.
TEST Z CHEMII I
ZADANIE 1
Dysponujesz wodnymi roztworami następujących soli:
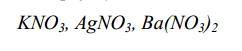
Korzystając z tablicy rozpuszczalności, wybierz spośród nich roztwór tej soli, za pomocą którego wytrącisz z wodnego roztworu chlorku glinu jony chlorkowe w postaci trudno rozpuszczalnego osadu. Napisz w formie jonowej skróconej równanie reakcji zachodzącej w czasie mieszania tych roztworów.
A. wzór odczynnika (wpisz wzór soli)
B. równanie reakcji w formie jonowej skróconej
ZADANIE 2
Narysuj wzór półstrukturalny (grupowy) jednego izomeru węglowodoru o wzorze sumarycznym C4H8 i podaj jego nazwę systematyczną.
ZADANIE 3
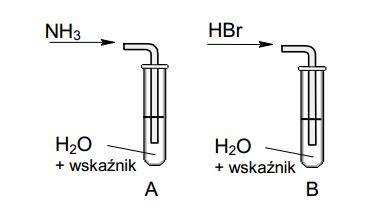
W celu zbadania zachowania gazowego amoniaku i bromowodoru wobec wody wykonano doświadczenia, które ilustruje poniższy rysunek.
Określ odczyn roztworów otrzymanych w obu probówkach.
Odczyn roztworu w probówce A
Odczyn roztworu w probówce B
ZADANIE 4
Podaj liczbę protonów i liczbę elektronów w jonie
ZADANIE 5
Wybierz poprawne sformułowanie.
Chlorku miedzi(II) nie można otrzymać działając
A. kwasem solnym na tlenek miedzi(II).
B. kwasem solnym na wodorotlenek miedzi(II).
C. kwasem solnym na miedź.
D. chlorem na miedź.
ZADANIE 6
Podaj, w jakiej kolejności i przy pomocy jakich metod wydzielisz chlorek sodu i piasek z mieszaniny piasku i wodnego roztworu chlorku sodu.
Najpierw wydzielam...
Następnie wydzielam...
Zastosowane metody...
ZADANIE 7
Podaj nazwę systematyczną związku o wzorze:
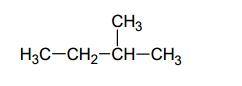
ZADANIE 8
Poniższy rysunek przedstawia doświadczenie, które wykonano w celu odróżnienia roztworu wodnego glukozy od roztworu wodnego glicerolu (gliceryny).
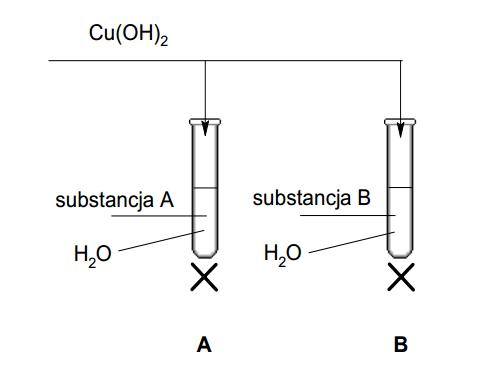
Przed ogrzaniem w obu probówkach niebieski osad wodorotlenku miedzi(II) rozpuścił się (roztworzył się) i powstał roztwór o szafirowym zabarwieniu. Po ogrzaniu w probówce A wytrącił się ceglasty osad, a w probówce B pojawił się osad o czarnym zabarwieniu.
A. Napisz, jaka cecha budowy cząsteczek glukozy i glicerolu (gliceryny) spowodowała powstanie szafirowego zabarwienia obu roztworów przed ich ogrzaniem.
B. Podaj nazwę substancji, której wodny roztwór znajdował się w probówce A i krótko uzasadnij swój wybór.
ZADANIE 9
Spośród podanych poniżej opisów reakcji chemicznych wypisz numery tych, którym ulegają aminokwasy.
1. Reakcja z kwasami prowadząca do otrzymania soli.
2. Reakcja z wodorotlenkami prowadząca do otrzymania soli.
3. Reakcja z wodą prowadząca do otrzymania polipeptydów.
4. Reakcja z aminokwasami prowadząca do otrzymania polipeptydów
ZADANIE 10
Ozon obecny w stratosferze (warstwie atmosfery położonej powyżej troposfery) pochłania szkodliwe promieniowanie ultrafioletowe. Zmniejszenie ilości ozonu w tej warstwie może mieć istotny wpływ na funkcjonowanie organizmów. Stężenie ozonu w troposferze (przyziemnej warstwie atmosfery) jest znacznie mniejsze niż w stratosferze. Wzrost ilości ozonu troposferycznego pozostaje w ścisłym związku ze wzrostem liczby przypadków astmy i problemów z układem oddechowym wśród populacji miejskiej.
Na podstawie: Peter O`Niell: Chemia środowiska, Warszawa 1997
Przeanalizuj przytoczony tekst i z poniższych zdań wybierz zdanie prawdziwe.
A. Zmniejszenie ilości ozonu stratosferycznego i wzrost ilości ozonu troposferycznego są zjawiskami pozytywnymi.
B. Zmniejszenie ilości ozonu stratosferycznego jest zjawiskiem pozytywnym, a wzrost ilości ozonu troposferycznego jest zjawiskiem negatywnym.
C. Zmniejszenie ilości ozonu stratosferycznego jest zjawiskiem negatywnym, a wzrost ilości ozonu troposferycznego jest zjawiskiem pozytywnym.
D. Zmniejszenie ilości ozonu stratosferycznego i wzrost ilości ozonu troposferycznego są zjawiskami negatywnymi.
ZADANIE 11
Uzupełnij zdania posługując się określeniami z poniższego zbioru: KCl, KNO3, nasycony, nienasycony, ochłodzić, ogrzać, dodać sól.
1. Solą lepiej rozpuszczalną w wodzie, w temperaturze 293 K jest ........
2. Rozpuszczając 60 g KNO3 w 100 g wody o temperaturze 313 K otrzymamy roztwór .........
3. W celu przeprowadzenia nasyconego roztworu KNO3 w roztwór nienasycony tej soli należy go ……
4. Aby wytrącić osad KCl z nasyconego roztworu tej soli należy ten roztwór ........
ZADANIE 12
Wskaż substancję pełniącą rolę utleniacza i rolę reduktora w procesie opisanym równaniem:
Zn + S → ZnS
Informacja do zadań 13 – 14
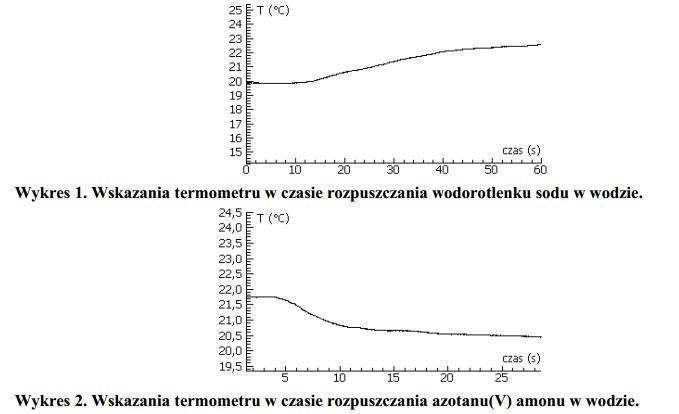
Przeprowadzono doświadczenie, w którym rejestrowano wartości temperatury podczas rozpuszczania wodorotlenku sodu, a następnie azotanu(V) amonu w wodzie. Rezultaty wykonanych pomiarów przedstawiają poniższe wykresy.
ZADANIE 13
Określ efekt energetyczny rozpuszczania w wodzie wodorotlenku sodu i azotanu(V) amonu. W tym celu uzupełnij następujące zdania.
Rozpuszczanie wodorotlenku sodu w wodzie jest procesem ......, ponieważ w czasie tego procesu temperatura .......
Rozpuszczanie azotanu(V) amonu w wodzie jest procesem ......, ponieważ w czasie tego procesu temperatura .....
ZADANIE 14
Spośród poniższych zdań wybierz to, które jest poprawnie sformułowanym wnioskiem na temat efektów energetycznych procesów rozpuszczania związków jonowych w wodzie, jaki można wyciągnąć na podstawie tego doświadczenia.
A. Na podstawie wyników tego doświadczenia nie można wnioskować o efekcie cieplnym rozpuszczania związków jonowych w wodzie, ponieważ wodorotlenek sodu i azotan(V) amonu nie są związkami jonowymi.
B. Rozpuszczaniu związków jonowych w wodzie zawsze towarzyszy wydzielenie ciepła.
C. Rozpuszczaniu związków jonowych w wodzie zawsze towarzyszy pochłonięcie ciepła.
D. Rozpuszczaniu związków jonowych w wodzie może towarzyszyć wydzielenie lub pochłonięcie ciepła.
ZADANIE 15
Wskaż nazwę procesu, który zajdzie, gdy do białka jaja kurzego dodamy alkohol etylowy.
A. Kondensacja
B. Denaturacja
C. Peptyzacja
D. Estryfikacja
Dołącz do nas na Facebooku!
Publikujemy najciekawsze artykuły, wydarzenia i konkursy. Jesteśmy tam gdzie nasi czytelnicy!
Dołącz do nas na X!
Codziennie informujemy o ciekawostkach i aktualnych wydarzeniach.
Kontakt z redakcją
Byłeś świadkiem ważnego zdarzenia? Widziałeś coś interesującego? Zrobiłeś ciekawe zdjęcie lub wideo?
